钜大LARGE | 点击量:507次 | 2019年02月18日
简述电池与燃料背后的简单化学
电池与燃料背后的简单化学


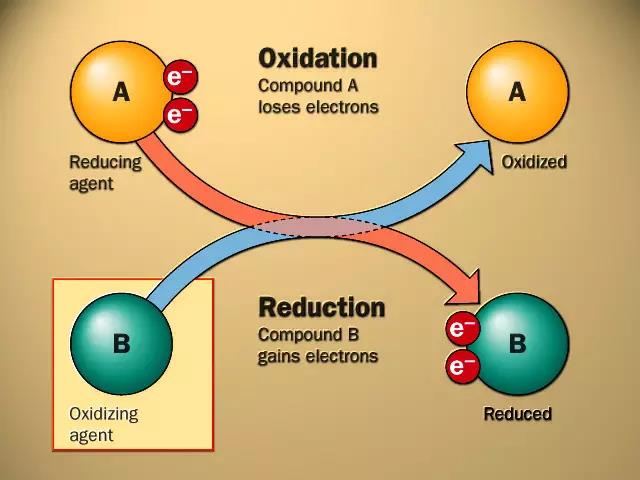
氧化还原


电池与燃料背后的简单化学
举几个例子:
1)H2-2e=2H+氢原子只有一个电子,全参与反应了,电子转移比是100%
2)Li-e=Li+锂原子有三个电子,只有一个参与反应,电子转移比是1/3=33%
3)Zn-2e=Zn(2+)锌原子有三十个电子,只有两个参与反应,电子转移比是2/30=6.7%
对于大多数物质,电子转移比例都很低,原因前面提到过。由此可见只有在元素周期表的前两行的轻原子有可能成为好的能量载体。前两行元素只有10个,氢氦锂铍硼,碳氮氧氟氖。其中氦与氖都是惰性气体,排除。氧与氟都是氧化剂,排除。氮大多数情况下都是准惰性气体,如果不是惰性气体要么毒死人要么熏死人,排除。我们还剩下5个元素,氢(100%),碳(66%),硼(60%),铍(50%),锂(33%)。
再进一步说,如果我们把一个原子当成电池的负极。那么这个半电池的能量密度(质量单位)可以用电子转移数与原子量来估算。如此以来,上面的比例将更为悬殊。还以氢作为基准:
碳(4/1233%)硼(3/10.828%),铍(2/9,22%)锂(1/7,14%)
大家很容易发现,最适合担任能量载体的两种元素分别是碳和氢,碳氢化合物,实际上就是我们生活中常见的汽油柴油煤油天然气等燃料。汽车选择这些高能量载体作为能量来源,已经是自然中的较优解了。电池跟各种碳氢化合物相比,可以说是天生不足。

























